各经销商:
根据《国家药监局关于修订复方感冒灵制剂和银黄口服制剂说明书的公告(2024年第81号)》要求,药品上市许可持有人(即我司)需于2024年9月27日前完成相关药品说明书修订及备案工作。现就我司银黄颗粒(国药准字Z20053526)说明书修订及后续执行事宜告知如下:
一、修订及备案情况说明
1、修订内容:
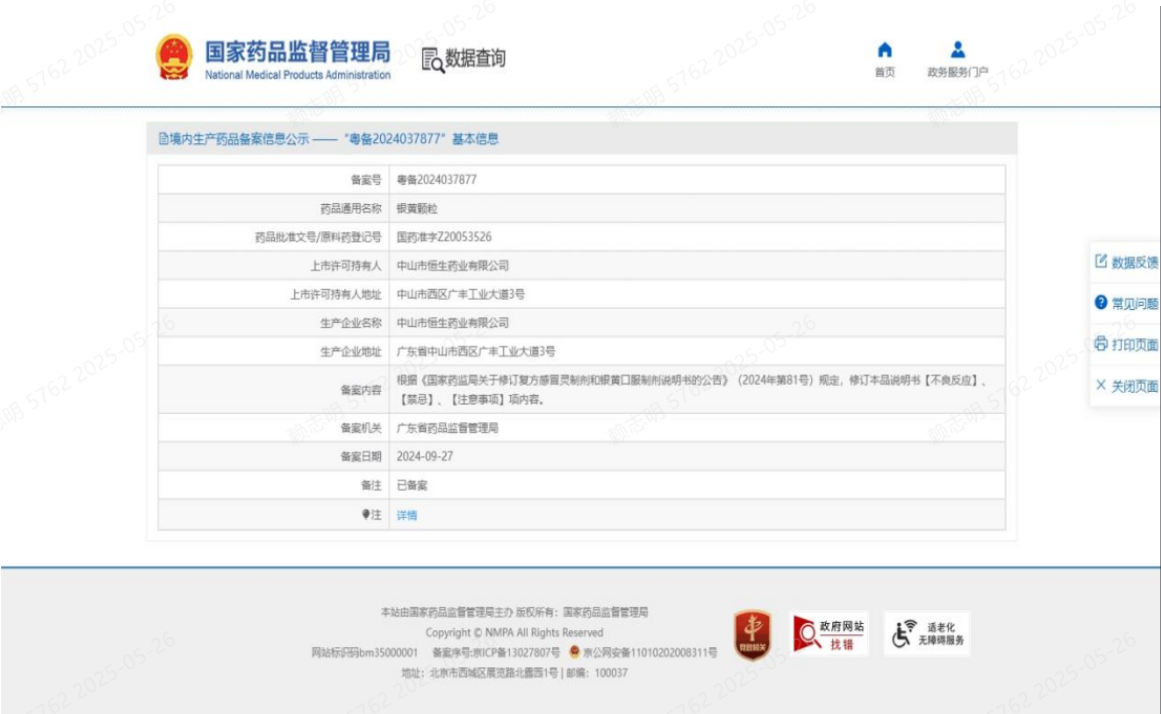
依据《国家药监局关于修订复方感冒灵制剂和银黄口服制剂说明书的公告(2024年第81号)》要求,我司已对银黄颗粒(国药准字Z20053526)药品说明书中【不良反应】、【禁忌】、【注意事项】项进行了修订,并于2024年9月27日通过广东省药品监督管理局备案(备案号:粤备2024037877号,详见附件1《备案证明》)。修订后的说明书符合《药品说明书和标签管理规定》(局令第24号)及现行法规要求。
二、患者告知与查询方式
为保障患者知情权及用药安全,我司已采取以下措施:
1、官方渠道公示:
修订后的说明书内容已通过我司官方网站(网址:https://www.zeus.cn/)说明书修订专栏公示,供公众查阅。
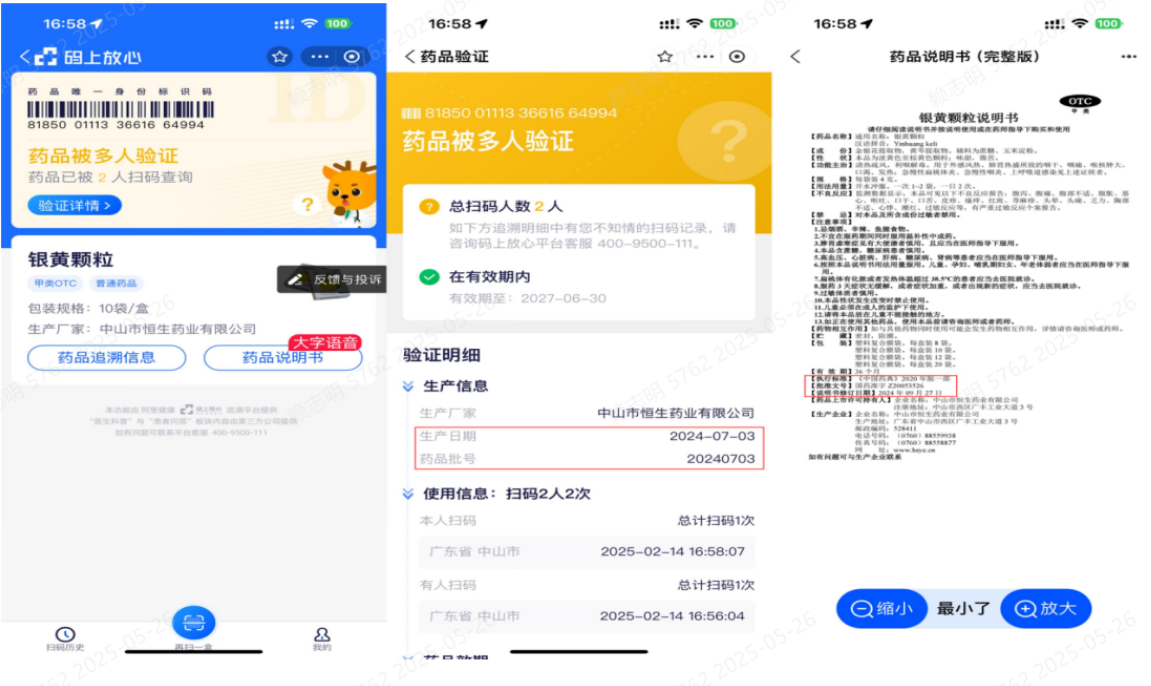
扫码查询:使用淘宝/支付宝扫描药品追溯码,进入页面后点击【药品说明书】栏目,即可查看完整版电子说明书(附件2为扫码操作指引)。
三、经销商协助事项
针对备案完成前已生产、使用旧版说明书的银黄颗粒库存产品,请贵司协助做好以下工作:
四、法律声明
本告知函内容符合《药品管理法》《药品说明书和标签管理规定》等法律法规要求,修订后的说明书已通过监管部门备案,具有法律效力。
附件:
1、备案证明
2、 扫码操作指引
中山市恒生药业有限公司
2025年5月26日
附件 1备案证明:
附件2:扫码操作指引
第一步:手机打开支付宝或淘宝,点击“扫一扫”,进入扫码页面

第二步:纸盒侧面找到“药品追溯码”

第三步:手机支付宝或淘宝扫码页面对“药品追溯码”进行扫码
第四步:进入码上放心平台,点击“药品说明书”
第五步:查看电子完整版药品说明书